Wie unsere Umwelt sind wir ständig ionisierender Strahlung aus überwiegend natürlichen Quellen ausgesetzt. Verliert ein Molekül ein Elektron, geht das entstandene Ion Reaktionen ein. Da erhebt sich sofort die Frage, wie die komplexen und daher verletzlichen biomolekularen Strukturen in lebenden Organismen solche zerstörerischen Effekte aushalten und überstehen können. Wie gehen organische Moleküle durch Ionisation kaputt und insbesondere wie beeinflussen und verändern nahe benachbarte Moleküle diese Prozesse?
Wissenschaftler um Alexander Dorn vom MPI für Kernphysik gehen diese Fragen experimentell an, indem sie Reaktionen gasförmiger organischer Moleküle mit den Reaktionen derselben Moleküle in Komplexen mit einem oder mehreren Partnern wie Wasser vergleichen. Schon früher fanden sie, dass nach Ionisation eines Wassermoleküls Energie vom Wasser auf das organische Molekül übertragen werden kann, was dieses ionisiert und zerbricht [Ren et al., Nature Physics, 2018]. In einer neuen Studie haben sie nun untersucht, was passiert, wenn das organische Molekül direkt ionisiert wird und sich dadurch möglicherweise verändert.
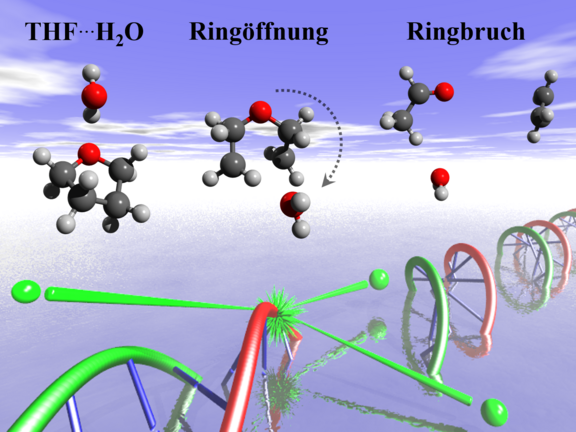
Der Gruppe gelang es, für biologisch relevante Paare (Dimere) aus zwei Tetrahydrofuran (THF) oder einem THF und einem Wassermolekül die zugrunde liegenden Mechanismen zu identifizieren. THF, ein fünfgliedriger Ring aus einem Sauerstoff- und vier Kohlenstoffatomen ähnlich wie die Desoxyriboseringe im Rückgrat der DNS, eignet sich als Modell um Strahlenschädigung der DNA zu studieren. „Wir haben einen Monomere, Dimere und auch größere Cluster enthaltenden Gasstrahl in einem Reaktionsmikroskop mit Elektronen beschossen und die übertragene Energie sowie gleichzeitig die Ionenmasse gemessen, um zu sehen, ob THF zerfallen ist“, erklärt Xueguang Ren, Post-Doktorand in der Gruppe von Alexander Dorn, die experimentelle Herangehensweise. Es zeigte sich, dass im Fall des geringstmöglichen Energieübertrags der THF-Ring in Dimeren zerbrach, während die Ringstruktur in einzelnen Molekülen wie auch in größeren Clustern intakt blieb.
Um tiefere Einblicke zu gewinnen haben die Wissenschaftler theoretische Berechnungen durchgeführt. „Augenblickliche Ionisation des organischen Moleküls verursacht eine plötzliche und starke Anziehung des benachbarten Wassermoleküls, das infolgedessen mit dem Ring zusammenstößt, was diesen zerbrechen lässt“, fasst Enliang Wang, ehemaliger Post-Doktorand in der Gruppe, die Ergebnisse zusammen. „Der Reaktionsweg verläuft über mehrere Zwischenstufen mit Protonentransfer als weiteren entscheidenden Schritt.“ Anders gesagt, wenn das THF in einem THF∙H2O-Dimer ionisiert ist, katalysiert das benachbarte Wassermolekül den Ringaufbruch.
Interessanterweise erfolgt diese Zerstörung nicht, wenn mehr als ein Wassermolekül gebunden ist, weil sich die Energie über viele Moleküle verteilen kann und dies eine effektive Kühlung darstellt. Die lokale wässrige Umgebung von Biomolekülen wirkt also als Schutzschild. „Unsere Resultate unterstreichen, wie wichtig es ist, die Energietransfer-Prozesse in kondensierte Materie zu verstehen, und dass die wässrige Umgebung in biologischen Zellen für die Stabilität von Biomolekülen bei Bestrahlung verantwortlich ist“, schlussfolgert Xueguang Ren.
Originalpublikation:
Water acting as a catalyst for electron-driven molecular break-up of tetrahydrofuran, Enliang Wang, Xueguang Ren, WoonYong Baek, Hans Rabus, Thomas Pfeifer, and Alexander Dorn, Nature Communications 04.05.2020, DOI: 10.1038/s41467-020-15958-7
Gruppe Dorn in der Abteilung Pfeifer